医疗新政下的外资进退之道:干细胞与基因治疗及独资医院领域的前景与挑战
医疗新政下的外资进退之道:干细胞与基因治疗及独资医院领域的前景与挑战
2024年9月7日,商务部、国家卫生健康委及国家药监局三部门联合发布了《关于在医疗领域开展扩大开放试点工作的通知》(以下简称“《医疗领域开放试点通知》”,后附中英文版通知全文),拟在医疗领域开展两项扩大开放试点工作,即自通知印发之日起,1)北京、上海、广东的自由贸易试验区及海南自由贸易港允许外商投资企业从事人体干细胞、基因诊断(CGT)与治疗技术的开发和应用以用于产品注册上市和生产;2)同时允许在北京、天津、上海、南京、苏州、福州、广州、深圳和海南全岛允许设立外商独资医院(不含中医和公立医院并购)。
在当今的经济大环境下,中国企业很难独善其身,很多外资企业也面临如何在中国发展的问题,是进是退,需谨慎考虑。借此次《医疗领域开放试点通知》,我们通过初步分析,为中外企业在中国的健康、长久发展提供一些思路。
一、政策和市场,支持中国迈向更深层次的市场开放
1、30年中国改革开放政策的支持
企业是微观的,国家政策是宏观的,企业生存、发展必然受到宏观政策的影响。回顾中国经济的发展,自1992年,中国确定了市场经济体制后,“引进来”就是一项基本国策;到2001年,中国加入WTO,稳步推动“走出去”“引进来”政策;而中国共产党第二十届中央委员会第三次全体会议后,会议公报重申了中国“必须坚持对外开放基本国策,坚持以开放促改革”的坚定决心,并将“稳步扩大制度型开放”置于了前所未有的战略高度。
“温故而知新”,从过去的30年时间看,中国是在一步一步,谨慎地拓宽开放的领域,推动经济的发展。从这个角度看,此次允许外商投资企业从事人体干细胞、基因诊断(CGT)与治疗技术的开发和应用,和设立外资医院,是在这个涉及到中国百姓民生的重要领域,迈出了改革开放的重要一步。
2、中国医疗市场稳定增长的支持
根据中国国家卫生健康委员会的统计,中国在医院数量,人均医疗费用支出都在稳定增长。仅以门诊诊疗人次和门诊费用情况为例,数据如下[1]:
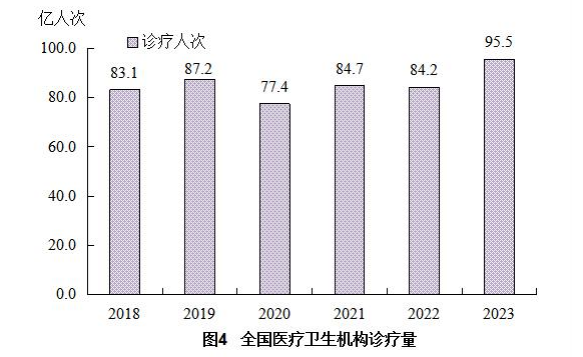
点击可查看大图
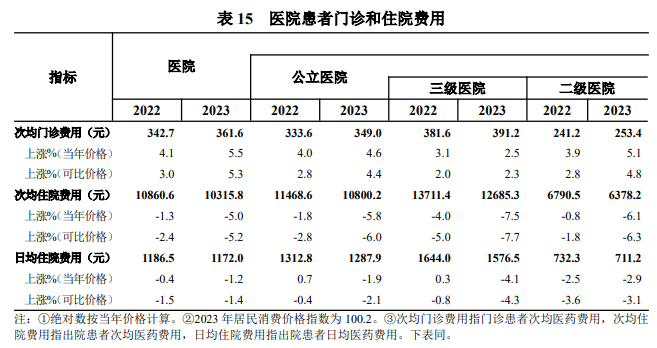
点击可查看大图
3、居民财务支持
根据中国人民银行发布的《2023年金融统计数据报告》,全年人民币存款增加了25.74万亿元,其中住户存款增加了16.67万亿元。进一步分析显示,中国居民存款余额在近8年内增长超过了一倍,从2016年的59.8万亿元增长到2023年的137万亿元。住户存款在总存款中的占比也从2016年的39.7%上升到了2023年的48.2%。[2]老百姓手中钱多了,随着人口老龄化、大众对健康的关注意识升高,在医疗卫生上的支出将会显著增加。
二、外资企业需要关注的重点问题
如果外资准备在中国投资这两个领域,那么就需要考虑以下问题。虽然我们2023年就陪同外资药企就靶向药物计划在中国做临床测试,拜访了中国相关部门沟通具体要求和制定商业方法等,但限于篇幅,在此不做非常具体的展开讨论,仅从法律角度对一些问题作提示,今后可以根据企业需要针对个案具体探讨。
1、入场程序:中国市场准入与策略
总结而言,在市场准入基础规则方面,在中国境内经营生物医药,需根据具体业务类型取得商务部、国家卫生健康委、国家药监局核准的对应药品资质。药品生产、销售商,需获取《药品生产许可证》、《药品经营许可证》等资质并通过药品生产/经营质量管理规范认证(GMP/GSP);在药品研发过程中,遵守《药品临床试验管理规范》(GCP);在药品研发完成后,需申请《药品注册证》;如涉及药品进出口的,则还需办理进出口企业相关工商、税务、海关、商检、外汇等备案登记流程。药品从研发到上市的基本过程包括但不限于研发筛选、临床前研究、临床研究、新药申报与审批、新药检测及生物等效性试验等,各个环节都需要遵守中国的严格监管规定。(这里就暂不对劳动、税务、工商管理等后续经营性问题做提示。)
由于干细胞与基因治疗高度专业化、创新性强,同时可能涉及到大量敏感数据及伦理问题,医药外资企业在该领域进行投资时应重点关注数据保护、数据跨境流动、人类遗传资源管理、知识产权、技术进出口等监管要求,如原先存在VIE架构的则还需要考虑架构是否拆除、投资结构调整优化的问题。
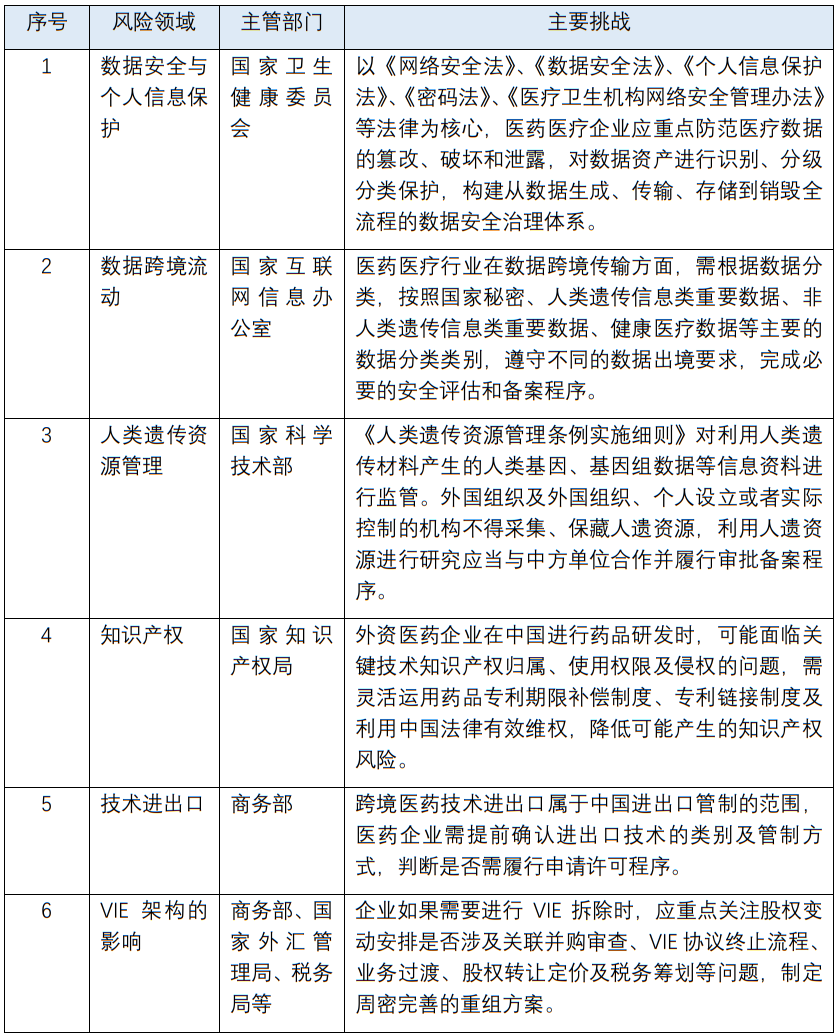
点击可查看大图
实务建议:中外市场因法律体系和具体规则的不同而存在差异,外资企业在进入中国市场前需提前关注制度差异,因地制宜制定具体投资方案。例如关注中外之间药品专利保护机制的差异等,以提前形成对于现有成果有效保护的专利组合。很多外资在拓展中国市场的过程中,采取“小步快跑”的模式,逐步推进。在开发客户的同时,与中国各监管机构建立起成熟有效的沟通机制,为此后业务推进和创新打好基础。
2、外资医药企业的挑战:美国生物及数据安全立法的影响
除需考虑中国方面的市场准入挑战外,外资医药企业投资中国也不得不考虑美国在生物及数据安全领域的行政令及立法草案的潜在影响。
从2018年美国就针对中国生物技术领域的发展制定相关的政策,2024年9月9日,美国《生物安全法案》(The Biosecure Act, H.R.8333)在众议院获得通过,未来几个月将在参议院进行审议,该法案拟限制美国政府及其实际控制的公司与特定生物技术公司签订合同,并对敏感数据的获取和传输进行了限制。结合此前美国已经生效的第14117号行政命令《关于防止受关注国家访问美国人的大量数据和美国政府相关数据的行政命令》及《2024年保护美国人数据免受外国敌对势力法》,美国目前已确立了部分针对敏感数据获取的限制规则,中国(含香港和澳门)在获取美国人敏感个人数据包括但不限于特定种类的个人识别信息、生物特征识别信息、人类组学数据、个人健康数据等时将受到限制乃至禁止。所以外资企业需要结合自身产品情况、研发情况、商业安排等,提前分析美国行政令及立法草案的潜在影响。
(就美国生物及数据安全立法的最新监管政策及要求,可参见我们之前的文章,《美国立法动向:制定“生物技术公司”的黑名单》及《下生物技术行业的多重风险因素》。)
实务建议:由于企业自身业务在中国和美国的发展,还有投资控股关系的因素等影响,外资企业在投资中国时,在合作对象、研发安排、技术引进时,有时不得不考虑其技术来源和被管控的情况。这需要企业提前做好方案,既稳妥挣钱,又避免合规问题。
三、结语
中国进一步开放,广阔的市场为企业提供了新的机遇。但医药产业具有高技术、高投入、高风险、高回报、长周期的特点,是典型的弱周期性行业。外资企业在中国医疗市场的收益不会在短时间内显现,希望我们的初步提示能够为外资企业期布局规划提供帮助,帮助外资企业应对中长期风险,稳步并可持续地在中国成长和收益。

扫描二维码可查看
附件:《商务部、国家卫生健康委、国家药监局关于在医疗领域开展扩大开放试点工作的通知》
[注]
[1] 中国国家卫生健康委员会规划发展与信息化司,《2023年我国卫生健康事业发展统计公报》,http://www.nhc.gov.cn/guihuaxxs/s3585u/202408/6c037610b3a54f6c8535c515844fae96.shtml
[2] 和讯网,《居民存款余额近8年增长超一倍,消费投资意愿下降,定期存款越来越受欢迎》,https://news.hexun.com/2024-05-17/212876718.html









