SPD模式在临床试验阶段的应用前景及合规要点前瞻
SPD模式在临床试验阶段的应用前景及合规要点前瞻
"SPD"全称为"Supply, Processing, Distribution",在医疗机构供应管理的语境下指"供应、分拣、配送",主要是指医疗机构所应用的一种供应链管理模式。SPD供应链管理目前在国内市场正处于成长阶段。有分析显示,按照全国3000家左右三级医院以及10000家左右二级医院的市场存量,以每家机构每次100万元采购系统的投入计算,SPD市场将超过百亿,再考虑到持续服务收费,以及和医药流通企业、医疗器械企业、医用耗材企业的合作,市场规模还会成倍放大。[1]同时,随着我国医药研发的发展,国内的临床试验正在快速发展,《中国新药注册临床试验进展年度报告(2021年)》显示,2021年,我国药物临床试验登记与信息公示平台登记的临床试验达3358项,较2020年增加29.1%,其中新药临床试验登记2033项,占比60.5%。随之而来的,在临床试验阶段引入SPD等管理模式以实现规模化与规范化的需求也持续增长。本文试图基于我国SPD行业发展现状,对SPD业务在临床试验阶段的应用及合规要点进行前瞻分析,以供行业相关人士参考。
一、SPD行业发展现状及在临床试验中的应用前景
1. SPD业务模式
2017年7月11日,国家卫生计生委办公厅等印发了《医用耗材专项整治活动方案》,提出"加强医疗机构医用耗材价格行为的监督检查……将主要医用耗材价格、总体用量、各科耗占比纳入院务公开范围……对于有条件的省份,应当将耗材集中采购价格等相关内容公开,接受社会监督。"等要求,进一步推动医疗机构采取引入SPD模式等措施以实现降本增效。
有别于传统的供应管理,SPD业务以信息物流技术为工具,对医疗机构内部物资管理的供应、分拣、配送三大环节进行一体化运营管理,其主要业务环节和流程如下图所示:
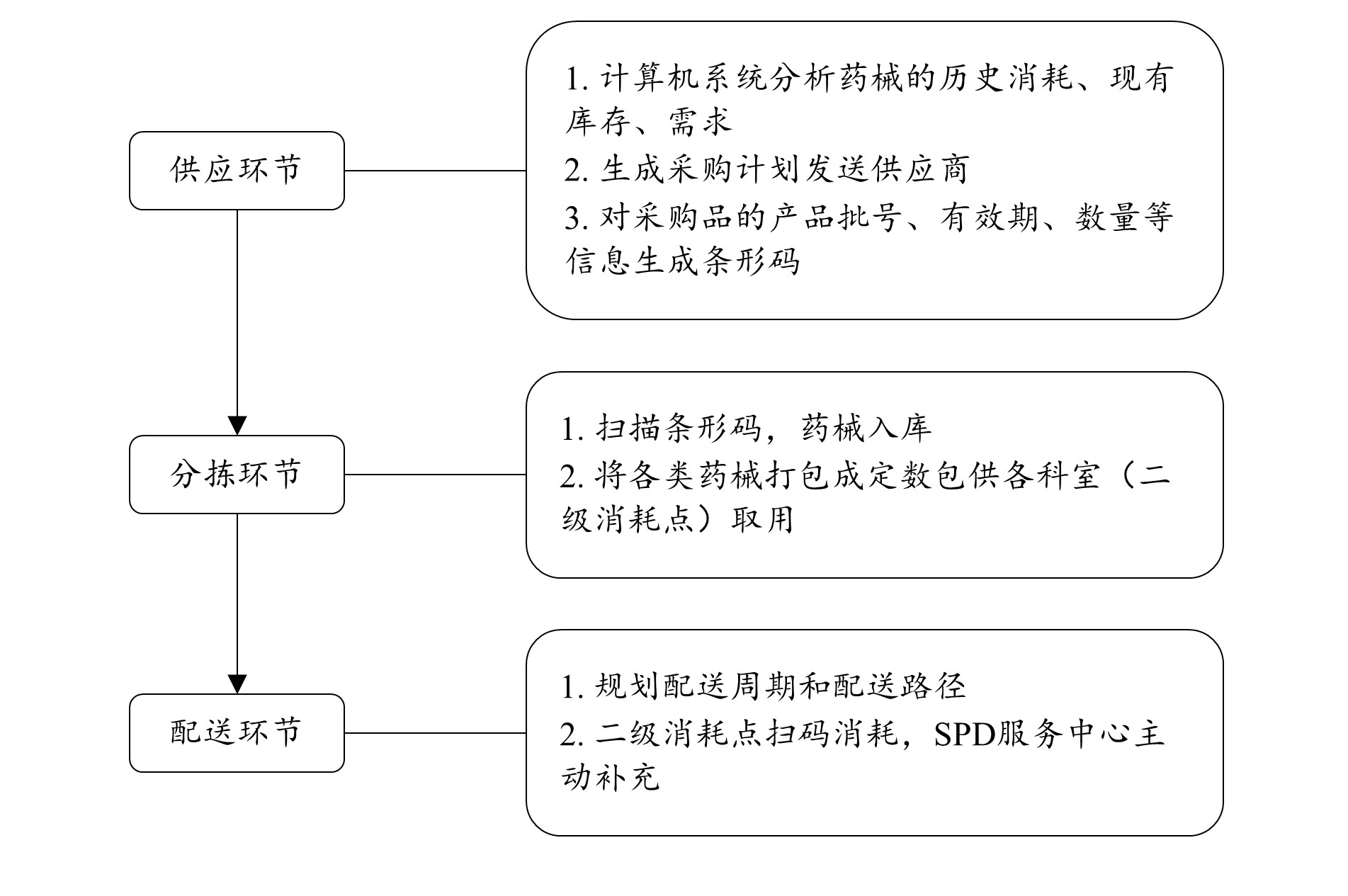
注:参见[2]
SPD业务在开展过程中,存在四种模式:
一是纯软硬件销售模式,医院直接购买纯软硬件产品;
二是医药商业公司集配模式,将医院的供应商归集到一家或几家,由其中一家进行SPD运营管理服务;
三是医药商业公司服务模式,由一家供应商为医院提供SPD运营管理服务,向其他供应商收取服务费;
四是纯第三方服务模式,由独立于医院与供应商的第三方SPD运营服务商提供SPD运营管理服务。
鉴于纯软硬件销售模式不涉及供应管理过程中的具体服务环节,因此本文讨论SPD业务主要聚焦于其余三种业务模式。
2. SPD业务发展现状
据中物联数据,目前全国有二级以上医院近1.4万家,已引进SPD项目的超过1000家,渗透率尚不足10%,SPD市场空间巨大。[3]2021年,中国物流与采购联合会医疗器械供应链分会对开展医疗器械SPD项目的488家公立医院进行调研统计分析。其中,开展医疗器械SPD项目的三级医院占比79%,三甲医院所占比例高达68%。医院类别主要以综合性医院为主,占比达85%。[4]
根据我们对公开披露信息的检索,已有多家医药上市公司在公告中披露其开展SPD业务的情况,列举如下:
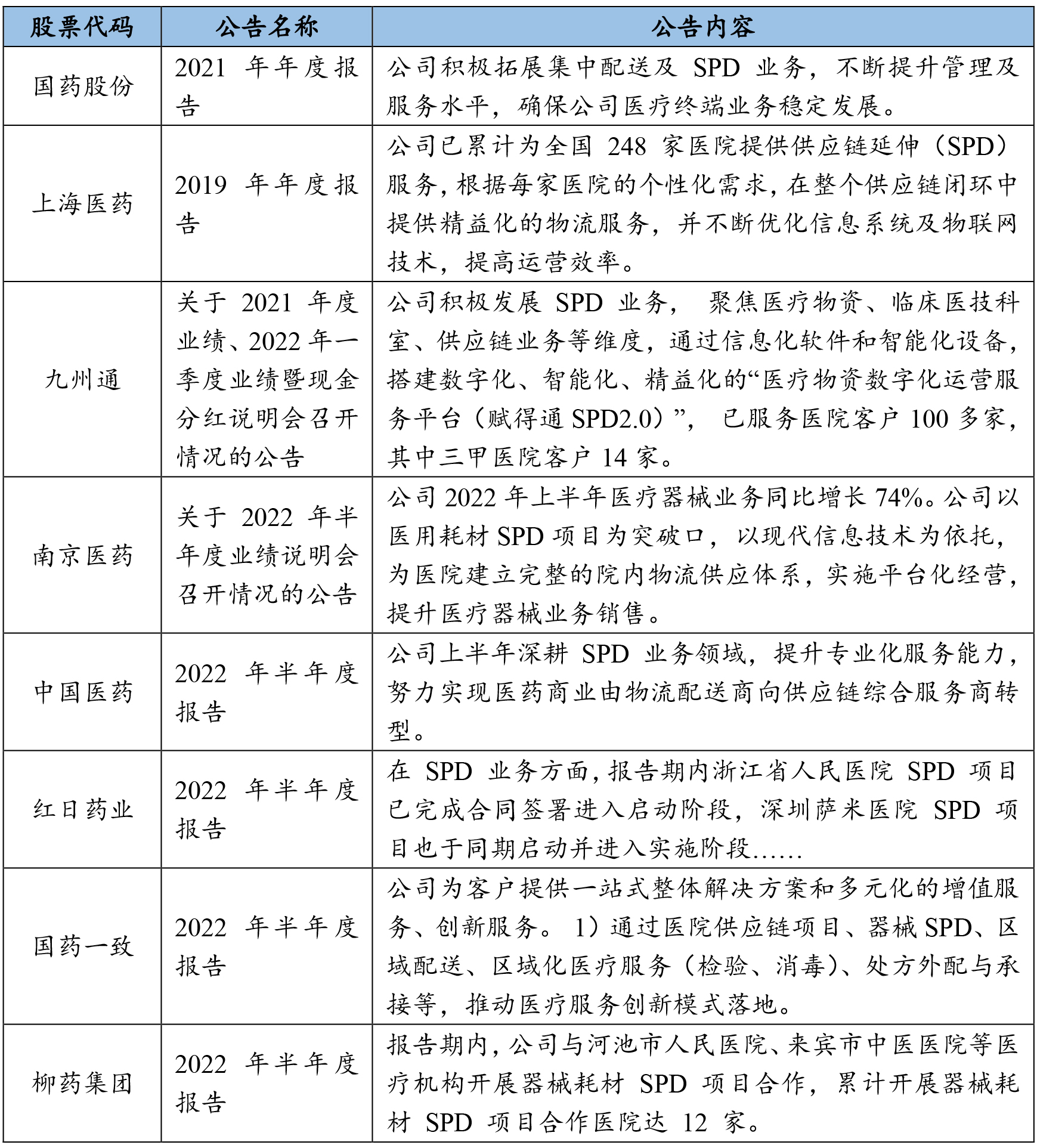
点击可查看大图
相比于SPD整体行业的快速发展,SPD行业中的细分领域——针对临床试验的SPD业务尚未广泛开展。在传统临床试验中,研究者除了需要实施临床试验之外,还需要兼顾药品或器械的采购及管理工作,例如药物或者样本的采购及储存、检测仪器的租赁及校准等。而这些物资的收发、存储、管理等还需要研究者兼顾医院整体的物资管理。这些临床试验药物供应和管理工作既繁复又琐碎,对研究者而言是时间的浪费,而对新药研发企业而言,其存在无法掌握相关渠道及管理能力的情形,可能导致临床试验因为药品供应的效率问题而影响进度。为了将研究者从繁重的后勤管理工作中解脱出来,并解决研发企业的临床试验药品供应管理的痛点,开展临床试验SPD业务具有了未来发展的前景。
二、临床试验SPD业务的合规要点
1. 院内仓库使用权的取得方式
在传统SPD业务的逻辑中,医院各科室作为二级消耗点,所需的药械来自于SPD模式下的一级仓库。由于医院对进入院内物流的管理较为严格,例如只在某一时段允许院外物资进入院内,一级仓库往往设在院内,以便及时调用。所以,SPD业务项下的院内仓库是否能够合法使用,是该业务是否可持续的核心。根据国家卫生计生委印发的《预算管理单位国有资产使用管理办法》,公立医院可以对外出租场地,但需要按照:6个月以内的出租自行审批,报国家卫生计生委备案;6个月(含)以上的出租依资产价值和医院性质的不同分别通过自行审批、上级主管部门审批、国家卫生计生委审批等,且存在需要根据《中华人民共和国招标投标法》以招标形式采购SPD供应商的情形。因此SPD服务提供商如需合法取得院内仓库的使用权,本身即需要以医院取得上述审批备案程序及/或履行招投标为前提,由医院作为SPD服务的接受方及付费方。
但在针对临床试验的SPD业务模式中,推动临床试验及承担相应成本的是临床试验的申办者,而申办者(尤其是中小医药研发企业)因其本身的资质以及并无长期使用院内仓库的需求,其无能力且无动力主动取得院内仓库使用权;对应的,临床试验SPD服务提供商为提高其服务效率及深度,存在取得院内仓库使用权的需求时,则需通过前述合规程序取得院内仓库使用权。但是,考虑到临床试验用药本身占医院药品使用量的比例很低且仓库使用需求与研究者承接临床试验的数量频次相关,其自身很难直接取得院内仓库使用权,故可能需要通过与现有SPD服务商之间的合作而取得使用权。但是,传统SPD服务商通过招标流程取得医院内部场地,若转交给临床试验SPD服务提供者管理后,可能存在违反《中华人民共和国招标投标法》第四十八条的风险(即中标人不得向他人转让中标项目,也不得将中标项目肢解后分别向他人转让)。
因此,临床试验SPD业务涉及使用院内仓库需求的,需要关注取得方式的合规性,提前论证相关业务开展所涉院内仓库使用权取得审批手续的可行性,以及在合作情形下避免被认定为中标项目转让的风险。
2. 管理人员的资质
根据《药物临床试验质量管理规范》第二十一条,研究者和临床试验机构对申办者提供的试验用药品有管理责任,研究者和临床试验机构应当指派有资格的药师或者其他人员管理试验用药品。因此,临床试验用药品应由"药师"或"其他人员"管理。
根据《执业药师注册管理办法》第三条,"药师"是指持有《中华人民共和国执业药师职业资格证书》并经注册取得《中华人民共和国执业药师注册证》后以执业药师身份执业的人员。
但《药物临床试验质量管理规范》并未对有资格管理临床试验用药品的"其他人员"作出定义,《执业药师注册管理办法》也没有此类表述,只有《中华人民共和国药品管理法》中存在"其他药学技术人员"这一相近概念,但也没有作出定义。我们认为,此处的"其他人员"至少应与"药师"在资格方面具有相当性。
因此,除了仅提供软硬件服务的模式不涉及人员之外,在医药商业公司或其他第三方提供临床试验SPD服务的情况下,尤其是对于医药商业公司之外仅有物流背景的第三方而言,出于合规性的考虑,建议聘用至少具有药师资格的人员对试验用药品进行管理。
3. 研究者的反向选择
在仅面向医院常规诊疗服务的SPD业务中,SPD服务提供者与医院分别作为供需双方。但在临床试验SPD业务中,出现了三个角色:SPD服务提供者、申办者(作为SPD服务购买者)、研究者(作为SPD服务实际体验者)。
在三角关系中,申办者虽然购买了SPD服务,但无法直接体验到服务质量。临床试验所需的样本、药物、器械的提供是否及时,仪器设备调试是否精准,是研究者能在临床试验开展中才能有直观感受的。因此研究者会对选用哪一家SPD服务提供者产生偏好,并将这一偏好传导至研究者,从而反过来决定该临床试验选用哪一家SPD服务提供者。随着在某一固定临床试验机构开展SPD服务的次数增加,SPD服务提供者与研究者或者其所在的临床试验机构的合作互信程度加深,二者逐渐形成一种绑定关系:申办者若是想要与该研究者或该临床试验机构合作开展临床试验,则不得不选择某一特定的SPD服务提供者。
如果因为某一家或某一些临床试验机构在某一领域的专长、拥有独占的病源等优势,导致想要开展某类临床试验的申办者不得不选择该临床试验机构,但同时,这家或这些临床试验机构都偏好同一家SPD服务提供者,则申办者往往不得不购买这家SPD服务提供者的服务。这种情形与《中华人民共和国反垄断法》第十七条所禁止的具有市场支配地位的经营者进行没有正当理由的搭售或在交易时附加其他不合理的交易条件存在相似之处。尽管如此,临床试验协议下,临床试验机构是否可被认定为经营者有待探讨,在临床试验SPD业务发展到一定阶段后,是否会触及《反垄断法》项下的规制还有待实践进一步观察。
4. 现有监管空白
经查询相关法律法规,尚无直接针对临床试验SPD的监管要求。根据我们向相关药监部门的了解,对于开展临床试验药品供应、分拣、配送的业务,目前没有审批或备案的监管要求,也没有出台过相关政策或指引。但是,以面向医院常规诊疗服务的SPD业务作为参考,2019年,广东省卫健委曾发布消息叫停SPD。当时广东省内223家医疗机构主要以医药物流供应链延伸的方式与广药、国控、华润、上药等企业签订合作协议,但由于药品供应链延伸还存在着一些自身难以克服的问题而被叫停。
现阶段临床试验SPD行业尚处于发展初期,法律监管暂时处于空白阶段,但鉴于医药行业关于人民身体健康属性具有强监管的特点,在未来临床试验SPD行业发展之后,相关政策法规可能会趋于明确以填补目前的监管空白,将临床试验SPD业务纳入常态化的监管。
三、结语
目前,临床试验SPD业务具有市场需求和发展前景,但对于有意向参与其中的企业来说,除了商业模式的考量之外,还需要考虑到不同的商业模式所牵涉潜在合规风险的差异。随着临床试验SPD业务开展的逐渐增多,相信相关监管法规也会逐渐完善,临床试验SPD将趋于良性发展,从而更好地促进临床试验以及我国药品研发产业的长远发展。
[注]










